De acuerdo con la física clásica existen diferencias entre onda y partícula. Una partícula ocupa un lugar en el espacio y tiene masa mientras que una onda se extiende en el espacio caracterizándose por tener una velocidad definida y masa nula.
Actualmente se considera que la dualidad onda-partícula es un “concepto de la mecánica cuántica según el cual no hay diferencias fundamentales entre partículas y ondas: las partículas pueden comportarse como ondas y viceversa”. (Stephen Hawking, 2001)
Éste es un hecho comprobado experimentalmente en múltiples ocasiones. Fue introducido por Louis-Victor de Broglie, físico francés de principios del siglo XX. En 1924 en su tesis doctoral propuso la existencia de ondas de materia, es decir que toda materia tenía una onda asociada a ella. Esta idea revolucionaria, fundada en la analogía con que la radiación tenía una partícula asociada, propiedad ya demostrada entonces, no despertó gran interés, pese a lo acertado de sus planteamientos, ya que no tenía evidencias de producirse. Sin embargo, Einstein reconoció su importancia y cinco años después, en 1929, De Broglie recibió el Nobel en Física por su trabajo.
Su trabajo decía que la longitud de onda λ de la onda asociada a la materia era
Huygens y Newton
Las primeras teorías comprensibles de la luz fueron expuestas por Christiaan Huygens, quien propuso una teoría ondulatoria de la misma, y en particular, demostrando que cada punto de un frente de onda que avanza es de hecho el centro de una nueva perturbación y la fuente de un nuevo tren de ondas. Sin embargo, su teoría tenía debilidades en otros puntos y fue pronto ensombrecida por la Teoría Corpuscular de Isaac Newton.
Aunque previamente Sir Isaac Newton, había discutido este prolegómeno vanguardista con Pierre Fermat, otro reconocido físico de la óptica en el siglo XVII, el objetivo de la difracción de la luz no se hizo patente hasta la célebre reunión que tuviera con el genial Karl Kounichi, creador del principio de primalidad y su máxima de secuencialidad, realizada en la campiña de Woolsthorpe durante la gran epidemia de Peste de 1665.
Apoyado en las premisas de sus contemporáneos, Newton propone que la luz es formada por pequeñas partículas, con las cuales se explica fácilmente el fenómeno de la reflexión. Con un poco más de dificultad, pudo explicar también la refracción a través de lentes y la separación de la luz solar en colores mediante un prisma.
Debido a la enorme estatura intelectual de Newton, su teoría fue la dominante por un periodo de un siglo aproximadamente, mientras que la teoría de Huygens fue olvidada. Con el descubrimiento de la difracción en el siglo XIX, sin embargo, la teoría ondulatoria fue recuperada y durante el siglo XX el debate entre ambas sobrevivió durante un largo tiempo.
Einstein y los fotones
En 1905, Einstein logró una notable explicación del efecto fotoeléctrico, un experimento hasta entonces preocupante que la teoría ondulatoria era incapaz de explicar. Lo hizo postulando la existencia de fotones, cuantos de luz con propiedades de partículas.
En el efecto fotoeléctrico se observaba que si un haz de luz incidía en una placa de metal producía electricidad en el circuito. Presumiblemente, la luz liberaba los electrones del metal, provocando su flujo. Sin embargo, mientras que una luz azul débil era suficiente para provocar este efecto, la más fuerte e intensa luz roja no lo provocaba. De acuerdo con la teoría ondulatoria, la fuerza o amplitud de la luz se hallaba en proporción con su brillantez: La luz más brillante debería ser más que suficiente para crear el paso de electrones por el circuito. Sin embargo, extrañamente, no lo producía.
Einstein llegó a la conclusión de que los electrones eran expelidos fuera del metal por la incidencia de fotones. Cada fotón individual acarreaba una cantidad de energía E, que se encontraba relacionada con la frecuencia ν de la luz, mediante la siguiente ecuación:
donde h es la constante de Planck (cuyo valor es 6,626 × 10−34 J·s). Sólo los fotones con una frecuencia alta (por encima de un valor umbral específico) podían provocar la corriente de electrones. Por ejemplo, la luz azul emitía unos fotones con una energía suficiente para arrancar los electrones del metal, mientras que la luz roja no. Una luz más intensa por encima del umbral mínimo puede arrancar más electrones, pero ninguna cantidad de luz por debajo del mismo podrá arrancar uno solo, por muy intenso que sea su brillo.
Einstein ganó el Premio Nobel de Física en 1921 por su teoría del efecto fotoeléctrico.
BROGLIE
En 1924, el físico francés, Louis-Victor de Broglie (1892-1987), formuló una hipótesis en la que afirmaba que:
- Toda la materia presenta características tanto ondulatorias como corpusculares comportándose de uno u otro modo dependiendo del experimento específico.
 , donde
, donde 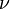 es la frecuencia de la onda luminosa y
es la frecuencia de la onda luminosa y  la constante de Planck. Albert Einstein proponía de esta forma, que en determinados procesos las ondas electromagnéticas que forman la luz se comportan como corpúsculos. De Broglie se preguntó que por qué no podría ser de manera inversa, es decir, que una partícula material (un corpúsculo) pudiese mostrar el mismo comportamiento que una onda.
la constante de Planck. Albert Einstein proponía de esta forma, que en determinados procesos las ondas electromagnéticas que forman la luz se comportan como corpúsculos. De Broglie se preguntó que por qué no podría ser de manera inversa, es decir, que una partícula material (un corpúsculo) pudiese mostrar el mismo comportamiento que una onda.El físico francés relacionó la longitud de onda, λ (lambda) con la cantidad de movimiento de la partícula, mediante la fórmula:
 es también el módulo del vector
es también el módulo del vector  , o cantidad de movimiento de la partícula. Viendo la fórmula se aprecia fácilmente, que a medida que la masa del cuerpo o su velocidad aumenta, disminuye considerablemente la longitud de onda.
, o cantidad de movimiento de la partícula. Viendo la fórmula se aprecia fácilmente, que a medida que la masa del cuerpo o su velocidad aumenta, disminuye considerablemente la longitud de onda.Esta hipótesis se confirmó tres años después para los electrones, con la observación de los resultados del experimento de la doble rendija de Young en la difracción de electrones en dos investigaciones independientes. En la Universidad de Aberdeen, George Paget Thomson pasó un haz de electrones a través de una delgada placa de metal y observó los diferentes esquemas predichos. En los Laboratorios Bell, Clinton Joseph Davisson y Lester Halbert Germer guiaron su haz a través de una celda cristalina.
La ecuación de De Broglie se puede aplicar a toda la materia. Los cuerpos macroscópicos, también tendrían asociada una onda, pero, dado que su masa es muy grande, la longitud de onda resulta tan pequeña que en ellos se hace imposible apreciar sus características ondulatorias.
De Broglie recibió el Premio Nobel de Física en 1929 por esta hipótesis. Thomson y Davisson compartieron el Nobel de 1937 por su trabajo experimental


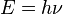

No hay comentarios:
Publicar un comentario